110932
论文已发表
注册即可获取德孚的最新动态
IF 收录期刊
- 3.4 Breast Cancer (Dove Med Press)
- 3.2 Clin Epidemiol
- 2.6 Cancer Manag Res
- 2.9 Infect Drug Resist
- 3.7 Clin Interv Aging
- 5.1 Drug Des Dev Ther
- 3.1 Int J Chronic Obstr
- 6.6 Int J Nanomed
- 2.6 Int J Women's Health
- 2.9 Neuropsych Dis Treat
- 2.8 OncoTargets Ther
- 2.0 Patient Prefer Adher
- 2.2 Ther Clin Risk Manag
- 2.5 J Pain Res
- 3.0 Diabet Metab Synd Ob
- 3.2 Psychol Res Behav Ma
- 3.4 Nat Sci Sleep
- 1.8 Pharmgenomics Pers Med
- 2.0 Risk Manag Healthc Policy
- 4.1 J Inflamm Res
- 2.0 Int J Gen Med
- 3.4 J Hepatocell Carcinoma
- 3.0 J Asthma Allergy
- 2.2 Clin Cosmet Investig Dermatol
- 2.4 J Multidiscip Healthc

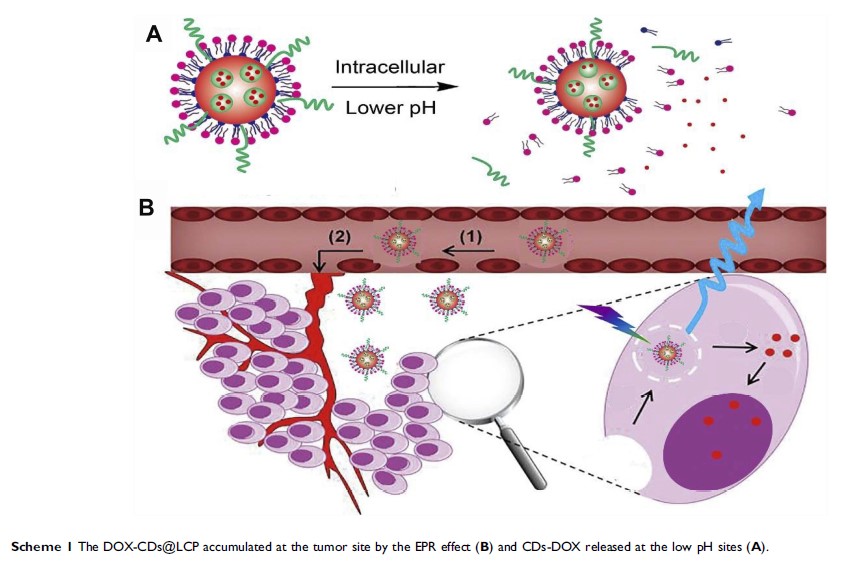
磷酸钙脂质体包裹的负载阿霉素碳点纳米颗粒为可视靶向肿瘤的递送和治疗
Authors Zhang J, Zhang H, Jiang J, Cui N, Xue X, Wang T, Wang X, He Y, Wang D
Received 29 August 2019
Accepted for publication 16 December 2019
Published 21 January 2020 Volume 2020:15 Pages 433—444
DOI https://doi.org/10.2147/IJN.S229154
Checked for plagiarism Yes
Review by Single-blind
Peer reviewer comments 2
Editor who approved publication: Dr Linlin Sun
背景:近年来碳点(Carbon dots, CDs)因具有良好的生物相容性和独特的光学性能受到了广泛的关注。但是以其较低的 pH 敏感性,在应用药物传递系统中,它们不能很好地分布于肿瘤部位。这是药物输送的障碍。碳点与阿霉素(DOX)结合包裹脂溶性磷酸钙(LCP)的纳米颗粒作为一种合适的成像物,用于 pH 敏感性纳米载体和抗肿瘤药物的递送。
材料与方法:利用柠檬酸和乙二胺采用一步水热处理法制备碳点。采用微乳液法制备纳米粒粒制备磷酸钙(CaP)芯并进一步包裹阳离子脂质。
结果:用红外光谱、x 射线衍射、透射电镜对其结构进行了表征。体外释放研究结果表明,DOX-CDs@LCP 与 pH 值有关。细胞毒性实验证实了这一点与对照组 (DOX-CDs) 相比,表现出更高的效率,但弱于自由组阿霉素。细胞摄取表明这些 pH 敏感的纳米颗粒可以有效地将 DOX 摄取到细胞质,达到抗肿瘤的效果。荧光成像学显示,DOX-CDs@LCP 主要分布于肿瘤区域由于肿瘤的发生增强渗性和透保留效应 (EPR),并降低了系统毒性。重要的是,抗肿瘤活性研究表明,DOX-CDs@LCP 纳米粒子抗肿瘤活性高于其他各组且毒性较低。结果表明,由于 pH 反应,LCP 可显著促进肿瘤微环境的释放。DOX-CDs 能增强药物的载药能力,减少药物的过早释放,作为荧光成像的对比剂实时跟踪疗效。因此,DOX-CDs@LCP 具有抗肿瘤作用并降低肿瘤治疗的系统毒性。
结论:DOX-CDs@LCP 是一种有前途的肝癌化疗的肿瘤 pH 敏感性及影像定位的给药系统。
Keywords: carbon dots, calcium phosphate photodynamic therapy, pH-sensitive, bioimaging, tumor targeting, therapy